独特的设备识别技术可自动读取医疗ID和条形码
 17
17
 拍明芯城
拍明芯城
作者:Lisa Eitel
2013年,美国食品和药物管理局(FDA)实施了唯一设备识别系统或UDI规则。该规则旨在通过在制造、分销和使用点使用现代文档提供一致的医疗设备跟踪和识别方法,从而提高患者安全。与欧洲的医疗器械法规要求或其他国家的类似法规非常相似,美国 UDI 规则提高了报告准确性,并有助于在发生召回或不良事件时进行分析。
自 2023 年 9 月 24 日起,FDA 将在设备标签和包装上全面执行国家健康相关物品代码和药品代码。在此日期或之后贴上标签的任何医疗产品都必须完全符合 UDI 规定。该任务将影响以下方面:
3 类生命攸关产品,例如起搏器和植入假肢
2 类中等关键产品,例如注射器、导管和可吸收缝线
1 类低风险产品,例如牙线、医用服和氧气面罩
该指令的全面执行意味着,如果医疗设备没有可扫描的条形码,它将不再被视为有效/可用的产品,即使其上有人类可读的标签,即使该产品通常被认为是大多数用户很容易识别。此次全面实施将促进医疗行业和医疗保险计费的全面采用。

图 1:一些手持式直接零件标记 (DPM) 条形码验证器配备先进的照明和其他软件,可自动查找符号并循环设置,以优化对特定 DPM 标记和现有材料基材的读取。事实上,此处显示的LVS-9585可以验证 DPM 部件和打印标签,以进行全面分析和报告。 (图片来源:欧姆龙自动化)
签约实体(品牌持有者)负责
在美国,每个医疗产品的知识产权所有者和面向用户的品牌对 UDI 代码的准确性和质量负责。这一点尤其重要,因为医疗产品市场的大部分都是合同制造并外包给其他组织的设施。因此,承包组织有责任确保其整个供应链符合 UDI 要求并生产准确的标签。
独特的设备识别技术起源
UDI 是静态设备标识符。然而,包裹中物品数量的变化可能会触发对新标识符的需求。发行机构规定如何区分这些细节。同样,改变设备的包装无菌条件也可能改变设备标识符。更改设备的目标市场(将销售设备的国家/地区)、标签语言或 CE 标志也可能需要更改设备标识符。
在 UDI 规则出台之前,医疗器械制造商可能会在产品上贴上特定部件号的标签。经销商将在医疗保健提供者或医院再次更改该部件号之前更改该部件号。由于每个实体都可能在到达患者之前更改零件编号,因此几乎不可能高效地跟踪产品、处理召回、防止假冒或准确订购新库存。
相关:实施强大的可追溯性解决方案
目前,每台设备都会获得一个标准化且持久的标识符(称为 UDI),以便所有实体能够更快速、更精确地识别设备,最终减少医疗错误。该 UDI 是一个字母数字代码,包含两个关键数据:
设备标识符
生产标识符
设备标识符是分配给给定设备的静态标签,其中列出了贴标者(通常是设备制造商)和设备的特定型号。相反,生产标识符包含可能变化的数据,并且它可以包含的大部分数据是可选的。这些可能包括批次代码、序列号、有效期和生产日期。简而言之,可选数据可以是制造商或贴标商认为支持设备跟踪所必需的任何数据。
每个 UDI 标签必须以两种形式提供此信息:
人类可读的形式(纯文本)
机器可读形式(可通过条形码或 RFID 阅读器读取)
只要设备可以满足多种医疗应用,UDI 就必须直接标记在设备上,而不是在其包装上。该规则也适用于可以多次使用的设备。
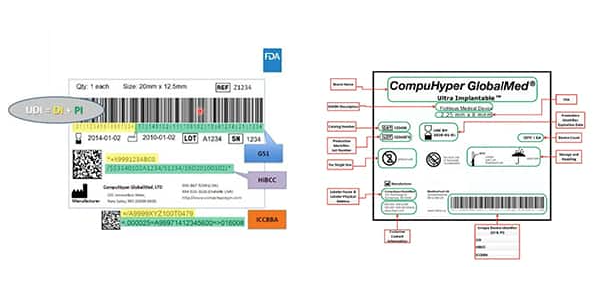
图 2:GS1、HIBCC 和 ICCBBA(UDI 发行机构)创建 UDI;分配 UDI 允许的符号系统;定义哪些技术可以与 UDI 交互;并规定UDI标志的质量要求。此示例中以黄色突出显示的是设备标识符;以绿色突出显示的是生产标识符。其他元素包括人类可读的信息……并且这些信息也被编码到机器可读的条形码中。 (图片来源:FDA)
所有设备都必须在全球 UDI 数据库中注册,以便在召回时进行跟踪,并使公众能够访问有关给定设备的信息。 FDA 认可的发证机构有权为设备制造商创建唯一标识符以放置在其产品上。
相关白皮书:保持最新的可追溯性
UDI扫描技术和技巧
UDI 标签从制造到使用的整个过程中可以通过多种方式进行验证。
在线验证是通过集成到大型机械中的技术来执行的,以便在生产时快速准确地处理大量产品。在先进软件的支持下,这些技术有时会采用工业级标签打印机的形式。这些打印机能够进行自己的内联验证,以确认 UDI 信息在标签生产时创建后立即可以按照严格的行业标准读取。例如,Omron Automation V275 验证器与 Zebra 热敏打印机配合使用,以符合 ISO 15426 和 FDA 合规性颁发机构GS1标准。
相关:欧姆龙追溯解决方案
在其他地方,在线验证采用自动化生产线上专门的机器视觉侧翼传送带的形式,结合条形码读取功能,可以极其快速、准确地验证高速生产线上的高混合产品上的 UDI 标签。 Omron Automation MicroHAWK产品在该领域表现出色,拥有先进的传感器,并辅以小型化结构和连接选项,包括以太网/IP 和 PROFINET。
相关:避免贴错标签的责任
相比之下,离线UDI验证最适合标签的批量抽样,以保证质量。离线验证通常用于医疗器械离开或到达设施时的样品测试,可以补充分销过程上游的在线验证系统。

图 3:直接标记在产品上的 UDI 需要的验证器与打印在粘贴标签上的 UDI 所使用的验证器不同。 (图片来源:欧姆龙自动化)
事实上,所有医疗配送和医疗保健运营都可以从使用符合 ISO 要求的验证器中受益。请考虑 Omron 的 LVS 95XX 系列离线 UDI 验证产品。这些人员被雇用:
在创建代码的激光打标站和标签打印机上
代码应用于产品时,产品可能独立于代码创建区域,也可能不独立
在质量控制站中确认模板、格式和其他代码元素
指定离线 UDI 验证程序变体
对于给定应用最合适的离线 UDI 验证器取决于几个参数。
条形码尺寸:大型条形码通常更容易使用具有由镜头焦距和传感器尺寸定义的大视野的标识符来扫描。考虑 Omron Automation 的 LVS-9510 桌面 UDI 标识符。该系列产品既可以读取线性标签,也可以读取二维标签。五个不同的版本各自具有不同的视野,因此设计人员可以选择与需要验证的条形码尺寸兼容的版本。拼接功能允许对超出视野的条形码进行分级。
此外,所有 LVS-9510 都可以自动确定评估代码以及识别和突出显示故障点所需的符号系统和孔径。

图 4:使用可验证线性 (1D) 和二维 (2D) 代码的设备,可以更轻松地满足 ISO 标准的条形码验证。一些此类设备确定评估代码以及识别和突出显示问题所需的符号系统和孔径。此处所示的 LVS-9510 具有拼接功能,可以对大于视场的条形码进行分级。 (图片来源:欧姆龙自动化)
条码类型:扫描仪必须读取由 HIBCC、ICCBBA 或(最常见的 2023 年)GS1 等发证机构分配的条码格式。 GS1 规定了 UPC、线性条形码和二维数据矩阵条形码的尺寸、格式和分辨率。
UDI 标记位置:考虑医疗器械的直接零件标记 (DPM)。这些标记可能非常小,特别是当它们识别手术器械和植入式医疗设备时。为了读取和验证此类 DPM UDI,Omron 的 LVS-9580 和 LVS-9585 超高密度手持式验证器配备了专用镜头,可以对无数 DPM 进行分级,包括单元尺寸小至 0.002 英寸的 DPM。LVS 内的工业级镜头-9580LVS-9585 确保一致的读取精度。最先进的是扫描仪内部高度可控和可校准的照明技术。除了多个视野之外,照明还可以立即优化捕获的 UDI 图像。这一点尤其重要,因为代码标准不允许事后更正或图像处理。
有关 UDI 扫描仪软件的更多信息
为了获得最大的有效性,支持验证器硬件的 UDI 软件必须以直观的格式呈现诊断信息。该软件必须根据 ISO 定义的参数对 UDI 代码进行分级(最重要的是确认其可读性),并且理想情况下还应该跟踪一系列 UDI 扫描中恶化的问题。
Omron 的每一款 UDI 扫描硬件都包含所有必要的软件。该软件定期更新,以跟上快速发展的法规和新的行业立法。
欧姆龙扫描仪软件的一个主要功能是处理代码语法。简而言之,每个条形码或二维码必须准确提取所有相关信息,包括产品类型、批号、适用数量、有效期、运输信息等。生成的数据字符串必须以特定方式格式化,以跟上不断变化的需求,方法论和医疗产品目的地。
扫描仪制造商定期更新的软件可确保最终用户即使在发布新代码时也能保持最新状态。
结论
美国军方曾计划全面采用像医疗行业UDI系统一样的UID产品追踪系统。其目的是减少军事设施中因丢失、重复和不计其数的物资而造成的大量浪费,这些物资包括从完整的雷神公司武器到由小型装备为某些特殊应用提供的控制板等一切物品。如今,UID 的使用程度参差不齐。
UDI 授权的命运不会相同。
推动 UDI 采用的口号很简单:标签就是产品。毕竟,不正确的标签可能会导致一系列事件,浪费医务人员的时间并导致医疗设备被丢弃。因此,UDI 必须出现在包装的所有层上,例如单元、包装、捆绑、箱子和托盘级别。灭菌密封内的无菌医疗器械上的 UDI 尤其重要,因为打破密封来验证器械类型是不可接受的。
随着 FDA 要求从 2023 年 9 月 24 日开始全面遵守 UDI 指令,用于验证医疗产品的先进扫描技术对于自动化制造商及其所服务的机器制造商和最终用户将变得至关重要。
此类扫描仪可以满足极为具体的 FDA UDI 要求,以确认各种实验室、医疗和临床诊断设备上的标签。离线条形码验证器最大限度地提高可追溯性、内联机器视觉和先进的 DPM 读取器。
责任编辑:David
【免责声明】
1、本文内容、数据、图表等来源于网络引用或其他公开资料,版权归属原作者、原发表出处。若版权所有方对本文的引用持有异议,请联系拍明芯城(marketing@iczoom.com),本方将及时处理。
2、本文的引用仅供读者交流学习使用,不涉及商业目的。
3、本文内容仅代表作者观点,拍明芯城不对内容的准确性、可靠性或完整性提供明示或暗示的保证。读者阅读本文后做出的决定或行为,是基于自主意愿和独立判断做出的,请读者明确相关结果。
4、如需转载本方拥有版权的文章,请联系拍明芯城(marketing@iczoom.com)注明“转载原因”。未经允许私自转载拍明芯城将保留追究其法律责任的权利。
拍明芯城拥有对此声明的最终解释权。




 产品分类
产品分类













 2012- 2022 拍明芯城ICZOOM.com 版权所有 客服热线:400-693-8369 (9:00-18:00)
2012- 2022 拍明芯城ICZOOM.com 版权所有 客服热线:400-693-8369 (9:00-18:00)


